proteína que facilita la reparación del ADN
Madrid, 15 de junio de 2021
Investigadores del CNIO
descubren que una proteína que facilita la reparación del ADN podría ser usada para potenciar la quimioterapia
- La proteína PrimPol ayuda a la célula a sobrevivir a las lesiones que causa la quimioterapia
- Los investigadores quieren hacer que las células tumorales sean más vulnerables a los tratamientos oncológicos reprimiendo en ellas PrimPol
- El Grupo de Replicación del ADN del CNIO, liderado por Juan Méndez, publica este trabajo en la revista The EMBO Journal
Juan Mendez Grupo replicacion del ADN
La quimioterapia mata a las células tumorales induciéndoles lesiones. Una de las más efectivas consiste en impedir que se separen las dos hebras de la molécula de ADN, de manera que la maquinaria celular no puede leer las instrucciones escritas en los genes. Pero a veces la célula logra reparar la lesión y sobrevivir, burlando el efecto de la quimioterapia. Investigadores del CNIO han descubierto cómo lo consigue, y planean usar ese conocimiento para potenciar los tratamientos oncológicos.
La clave está en una peculiar proteína llamada PrimPol, como explica en una publicación en The EMBO Journal el Grupo de Replicación del ADN del CNIO, liderado por Juan Méndez.
La molécula de ADN alberga los genes, que dirigen la vida de la célula y por extensión la de todo el organismo. Está compuesta por dos hebras entrelazadas, la famosa doble hélice. Para que las instrucciones escritas en los genes puedan ser leídas por la maquinaria celular, las dos hebras del ADN deben poder separarse y juntarse de nuevo, como una cremallera que se abre y cierra. Si esto no ocurre, la célula no puede funcionar ni, desde luego, replicarse.
Por eso las lesiones que impiden la separación de las hebras del ADN son de las más graves que puede sufrir una célula. Se llaman entrecruzamientos intercatenarios o ICLs, del inglés interstrand cross-links. Las lesiones ICL pueden aparecer de manera natural, por el propio metabolismo celular, o como consecuencia de determinados tóxicos, como en la quimioterapia. El cisplatino, usado en el tratamiento de los cánceres de ovario y pulmón, entre otros, elimina las células tumorales induciéndoles lesiones ICL.

El investigador que ha dirigido el estudio Juan Mendez en el centro junto a las investigadoras Elena Blanco Romero a la izquierda y Patricia Ubieto Capella a la derecha CNIO
Una ‘grapa’ encadenando la doble hélice
Como explica Méndez, “el ICL es un enlace químico entre las dos cadenas, una especie de grapa que impide su separación. Si la célula intenta dividirse, los cromosomas se terminan rompiendo”.
La célula, sin embargo, sabe reparar esas lesiones, que de hecho solo resultan letales cuando su frecuencia es muy alta. En el trabajo que ahora se publica en The EMBO Journal el grupo del CNIO desvela que lo logra en parte gracias a PrimPol.
PrimPol pertenece a una familia de proteínas llamadas “primasas” que apareció muy pronto en la evolución de la vida y hoy sigue presente en muchísimas especies, un indicio de su importancia para el funcionamiento de los organismos. En 2013, Juan Méndez y Luis Blanco, del Centro de Biología Molecular Severo Ochoa (CSIC), descubrieron por qué PrimPol es tan importante: permite a la maquinaria celular utilizar las instrucciones escritas en el ADN incluso cuando este contiene algún error. En otras palabras, PrimPol hace a la célula más resistente, la ayuda a sobrevivir cuando su ADN esté dañado.

Proteina ayuda a reparar el ADN y podria potenciar la quimioterapia
PrimPol ayuda a seguir leyendo el ADN
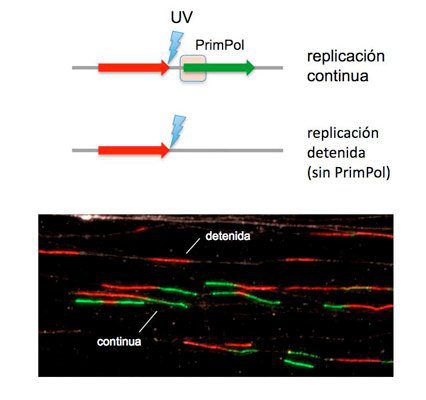
Normalmente las proteínas que copian el ADN se bloquean al detectar defectos en la doble hélice, y si el bloqueo es prolongado la célula acaba muriendo. Pero PrimPol consigue que la lectura del ADN se reinicie después del fallo, como un lector que sigue avanzando en un texto después de saltarse una palabra mal escrita o que no entiende. PrimPol, explica Méndez, ofrece “una solución inmediata” para evitar el bloqueo, dando a la célula la oportunidad de reparar el fallo en el ADN más adelante.
El nuevo trabajo se concentra en la función de PrimPol cuando el fallo es una lesión ICL. Los investigadores hallan que PrimPol es necesaria para la fase de copiado del ADN que precede a la reparación de la grapa en las hebras de ADN. Gracias a la participación de este enzima, la célula no solo sobrevive a las lesiones ICL, sino que además moviliza a la maquinaria encargada de repararlas.
cientificos espanoles identifican una enzima ancestral que facilita la reparacion del adn 1
Reprimir PrimPol para potenciar la quimio
Es un hallazgo básico, pero “con implicaciones clínicas muy interesantes”, dice Méndez, porque “al facilitar la reparación de ICLs, PrimPol está interfiriendo con la efectividad de la quimioterapia”.
Eso sugiere que si PrimPol no estuviera, la célula tumoral sería más sensible a la quimioterapia. Por eso los autores consideran que los nuevos resultados “abren la posibilidad de actuar contra PrimPol para potenciar los efectos terapéuticos de las moléculas que producen lesiones ICL”, escriben en EMBO Journal. proteína que facilita la reparación del ADN
En otro trabajo reciente en el que ha participado Méndez en colaboración con investigadores de Washington University (San Luis, EE.UU.) se ha hallado que las células tumorales de ovario producen más PrimPol para tolerar las lesiones en su ADN producidas por quimioterapia con cisplatino.
“Si conseguimos reprimir la función de PrimPol en estas células, podríamos mejorar la eficiencia de la quimioterapia”, señala Méndez. Para ello, su equipo está colaborando con el Programa de Terapias Experimentales del CNIO para identificar inhibidores específicos de PrimPol.
Anemia de Fanconi proteína que facilita la reparación del ADN
El nuevo trabajo también tiene interés para la anemia de Fanconi, una enfermedad poco frecuente pero muy grave. Los investigadores del CNIO demuestran que PrimPol facilita la reparación de las lesiones ICL por parte de una familia de proteínas llamadas FANC. Y son los fallos genéticos que reducen la actividad de esas proteínas los que causan la anemia de Fanconi.
“Los pacientes con anemia de Fanconi tienen muy pocas opciones terapéuticas, pero empieza a haber resultados muy prometedores con terapia génica”, afirma Méndez. “Todos los avances que permitan entender mejor las vías de reparación de ICLs pueden resultar útiles en un futuro próximo”.
El trabajo experimental ha sido llevado a cabo por tres estudiantes de doctorado dirigidos por Méndez: Daniel González, Elena Blanco y Patricia Ubieto. También han participado Luis Blanco, científico del CSIC, Massimo Lopes, científico de la Universidad de Zürich (Suiza), y la Unidad de Proteómica del CNIO.
El trabajo ha sido financiado por el Ministerio de Ciencia e Innovación, el Instituto de Salud Carlos III, el Fondo Europeo de Desarrollo Regional, la Fundación Nacional Suiza para la Ciencia y el Consejo Europeo de Investigación.
Artículo de referencia: PrimPol-mediated repriming facilitates replication traverse of DNA interstrand crosslinks. D. González-Acosta et al (The EMBO Journal, 2021). DOI: 10.15252/embj.2020106355.
CSIC, células que rodean los tumores,clave en la progresión del cáncer de mama



