WYSS, terapias de ARN, terapias celulares y diagnósticos
Los eToeholds son elementos de control diseñados que podrían hacer que las terapias de ARN sean más seguras, las terapias celulares más efectivas y permitir nuevas formas de biodetección.
28 de octubre de 2021 Por Benjamin Boettner
(BOSTON) – Los ARN se conocen mejor como las moléculas que traducen la información codificada en los genes en proteínas con su miríada de actividades. Sin embargo, debido a su complejidad estructural y relativa estabilidad, el ARN también ha atraído gran atención como un biomaterial valioso que puede usarse para crear nuevos tipos de terapias, biomarcadores sintéticos y, por supuesto, vacunas potentes, como hemos aprendido del COVID. -19 pandemia.
Creando un nuevo punto de apoyo para terapias de ARN, terapias celulares y diagnósticos
molécula de ARN sintético a una célula esencialmente le indica que produzca una proteína deseada, que luego puede llevar a cabo funciones terapéuticas, de diagnóstico y de otro tipo. Un desafío clave para los investigadores ha sido permitir que solo las células que causan o se ven afectadas por una enfermedad específica expresen la proteína y no otras. Esta capacidad podría agilizar significativamente la producción de la proteína en el cuerpo y evitar efectos secundarios no deseados.
Ahora, un equipo de biólogos sintéticos e ingenieros celulares dirigido por James J. Collins , Ph.D. en el Wyss Institute for Biologically Inspired Engineering y el Massachusetts Institute of Technology (MIT), ha desarrollado eToeholds: pequeños dispositivos versátiles integrados en el ARN que permiten la expresión de una secuencia que codifica una proteína enlazada solo cuando está presente un ARN viral o específico de una célula. Los dispositivos eToehold abren múltiples oportunidades para tipos más específicos de terapia de ARN, enfoques de ingeniería celular y de tejidos in vitro y la detección de diversas amenazas biológicas en humanos y otros organismos superiores. Los hallazgos se informan en Nature Biotechnology .
Puntos de apoyo para celdas superiores
En 2014 , el equipo de Collins, junto con el miembro de la facultad de Wyss Core, Peng Yin , Ph.D., desarrolló con éxito interruptores de apoyo para bacterias que se expresan en un estado apagado y responden a ARN desencadenantes específicos activando la síntesis de un proteína deseada por la maquinaria de síntesis de proteínas bacterianas. Sin embargo, el diseño de los dedos de los pies bacterianos no se puede utilizar en células más complejas, incluidas las células humanas, con su arquitectura más complicada y su aparato de síntesis de proteínas.
“En este estudio, tomamos elementos IRES [sitios de entrada de ribosomas internos], un tipo de elemento de control común en ciertos virus, que aprovechan la maquinaria de traducción de proteínas eucariotas, y los diseñamos desde cero en dispositivos versátiles que pueden programarse para detectar ARN desencadenante de células o patógenos específicos en células humanas, de levadura y de plantas ”, dijo Collins, miembro de la Facultad de Wyss Core. «EToeholds podría permitir enfoques terapéuticos y de diagnóstico de ARN más específicos y seguros, no solo en humanos, sino también en plantas y otros organismos superiores, y ser utilizados como herramientas en investigación básica y biología sintética». Collins también es profesor de Termeer de ingeniería médica y ciencia en el MIT.
Tomamos elementos IRES, un tipo de elemento de control común en ciertos virus, que aprovechan la maquinaria de traducción de proteínas eucariotas, y los diseñamos desde cero en dispositivos versátiles que se pueden programar para detectar ARN activadores específicos de patógenos o células en humanos, levadura y células vegetales.
Los elementos de control de IRES son secuencias que se encuentran en el ARN viral que permiten a los ribosomas que sintetizan proteínas de la célula huésped acceder a un segmento del genoma viral junto a una secuencia que codifica una proteína viral. Una vez que se adhieren al ARN, los ribosomas comienzan a escanear la secuencia que codifica la proteína, mientras que simultáneamente sintetizan la proteína agregando secuencialmente los aminoácidos correspondientes a su extremo de crecimiento.
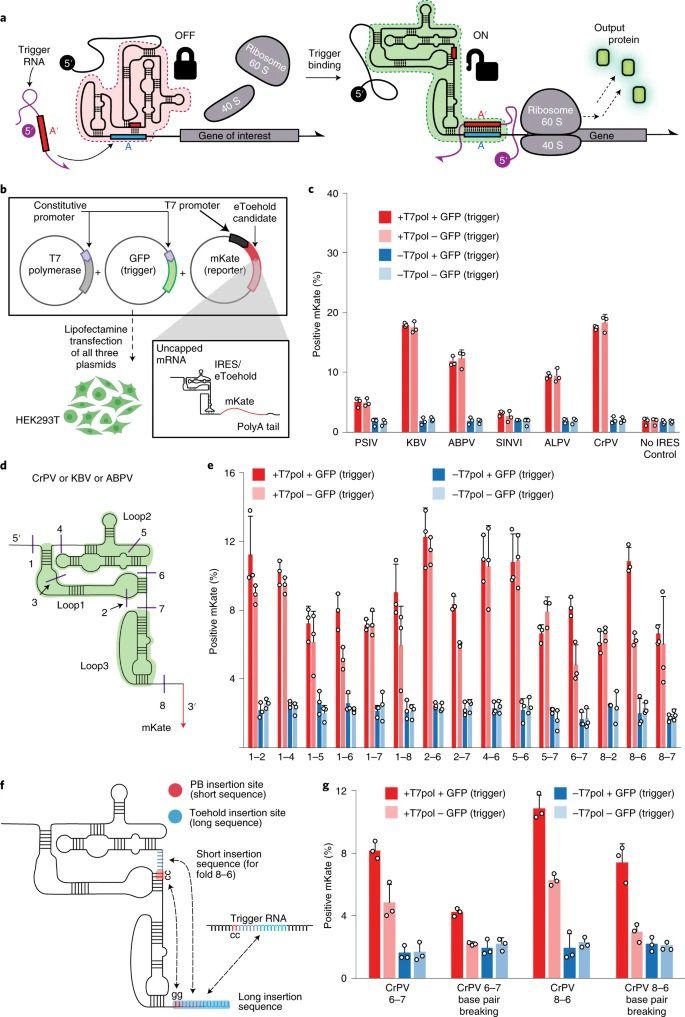
“Desarrollamos secuencias de IRES mediante la introducción de secuencias complementarias que se unen entre sí para formar estructuras inhibidoras de pares de bases, que evitan que el ribosoma se una al IRES”, dijo el coautor Evan Zhao, Ph.D., quien es un Becario postdoctoral en el equipo de Collins. “El elemento de secuencia que codifica el bucle de horquilla en eToeholds está diseñado de tal manera que se superpone con secuencias de sensor específicas que son complementarias a los ARN activadores conocidos. Cuando el ARN activador está presente y se une a su complemento en eToeholds, el bucle de horquilla se abre y el ribosoma puede encenderse para hacer su trabajo y producir la proteína «.
Zhao se asoció con el co-primer autor y becario de desarrollo tecnológico de Wyss, Angelo Mao , Ph.D., en el proyecto eToehold, que les permitió combinar sus respectivas áreas de experiencia en biología sintética e ingeniería celular para abrir nuevos caminos en la manipulación. de secuencias IRES.
Diseno y cribado de eToehold
En un proceso de iteración rápida, pudieron diseñar y optimizar eToeholds que eran funcionales en células humanas y de levadura, así como ensayos de síntesis de proteínas sin células. Lograron una inducción hasta 16 veces mayor de genes indicadores fluorescentes vinculados a eToeholds exclusivamente en presencia de sus ARN desencadenantes apropiados en comparación con los ARN de control.
“We engineered eToeholds that specifically detected Zika virus infection and the presence of SARS-CoV-2 viral RNA in human cells, and other eToeholds triggered by cell-specific RNAs like, for example, an RNA that is only expressed in skin melanocytes,” said Mao. “Importantly, eToeholds and the sequences encoding desired proteins linked to them can be encoded in more stable DNA molecules, which when introduced into cells are converted into RNA molecules that are tailored to the type of protein expression we intended. This expands the possibilities of eToehold delivery to target cells.” WYSS, terapias de ARN, terapias celulares y diagnósticos WYSS, terapias de ARN, terapias celulares y diagnósticos
Los investigadores creen que su plataforma eToehold podría ayudar a dirigir las terapias de ARN y algunas terapias génicas a tipos de células específicos, lo cual es importante ya que muchas de estas terapias se ven obstaculizadas por toxicidades excesivas fuera del objetivo. Además, podría facilitar los enfoques de diferenciación ex vivo que guían a las células madre a lo largo de las vías de desarrollo para generar tipos celulares específicos para terapias celulares y otras aplicaciones. La conversión de células madre y células intermedias a lo largo de muchos linajes de células diferenciadoras a menudo no es muy eficaz, y eToeholds podría ayudar a enriquecer los tipos de células deseados.
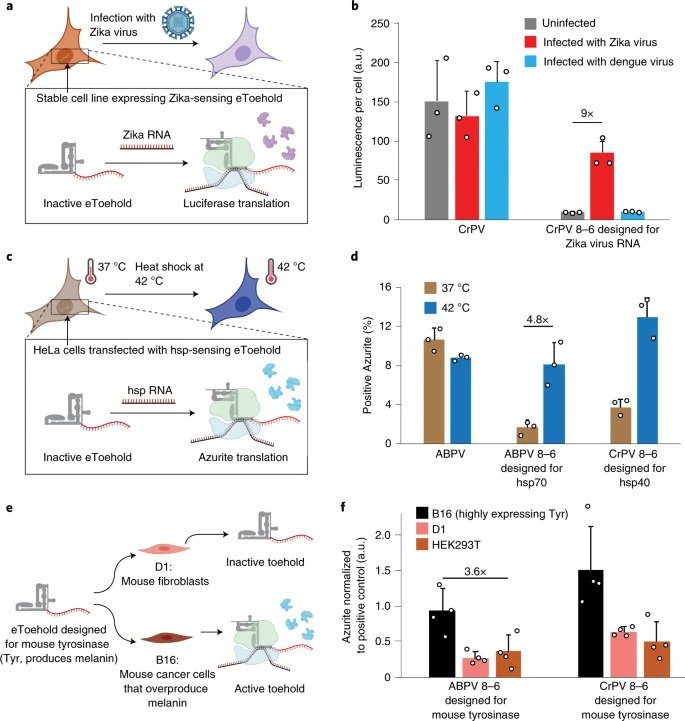
a , Se crearon líneas celulares estables con módulos eToehold diseñados para detectar la infección por el virus del Zika. b , Señal luminiscente de células diseñadas para expresar nanoluciferasa tras la infección por Zika después de una infección simulada, por Zika o por dengue. Las células diseñadas con nanoluciferasa activada por CrPV se utilizaron como control positivo. c , línea celular estable creada con módulos eToehold diseñados para detectar la exposición al calor mediante la detección de ARNm de proteína de choque térmico. d , las células HeLa se transfectaron con construcciones que contenían un indicador de GFP y azurita activada por eToehold. e , Se transfectaron construcciones diseñadas para traducir la proteína Azurita en presencia de Tyr de ratón en células B16, D1 o HEK293T (no mostradas). F, Expresión de azurita activada por eToehold en células B16, D1 o HEK293T después de la transfección. Los datos se presentan como valores medios con barras de error que representan la desviación estándar de tres réplicas técnicas (cuatro en la Fig. 3f ) expuestas a las mismas condiciones. Todos los experimentos fueron repetidos al menos tres veces. hsp, proteína de choque térmico.
“Este estudio destaca cómo Jim Collins y su equipo de Wyss Living Cellular Device Platform están desarrollando herramientas innovadoras que pueden avanzar en el desarrollo de terapias celulares y de ARN más específicas, seguras y efectivas, y tener un impacto tan positivo en la vida de muchos pacientes, ”Dijo el director fundador de Wyss, Donald Ingber , MD, Ph.D., quien también es profesor de Biología Vascular Judah Folkman en la Escuela de Medicina de Harvard y el Hospital de Niños de Boston, y profesor de Bioingeniería en la Escuela de Ingeniería y Aplicación de Harvard John A. Paulson Ciencias. WYSS, terapias de ARN, terapias celulares y diagnósticos WYSS, terapias de ARN, terapias celulares y diagnósticos
Otros autores del estudio son Helena de Puig, Ph.D., Kehan Zhang, Ph.D., Nathaniel Tippens, Ph.D., Xiao Tan, MD, F. Ann Ran, Ph.D., Asistente de investigación de Wyss Isaac Han, Peter Nguyen, Ph.D., Emma Chory, Ph.D., Tiffany Hua, Pradeep Ramesh, Ph.D., Wyss Staff Scientist David Thompson, Ph.D., Crystal Yuri Oh, Eric Zigon y Max English . El estudio fue financiado por subvenciones de BASF, los NIH (bajo la subvención # RC2 DK120535-01A1) y el Instituto Wyss de Ingeniería de Inspiración Biológica.