Un mal grupo
Las células tumorales a menudo hacen metástasis en grupos con otras células, lo que ofrece nuevas dianas para los tratamientos.

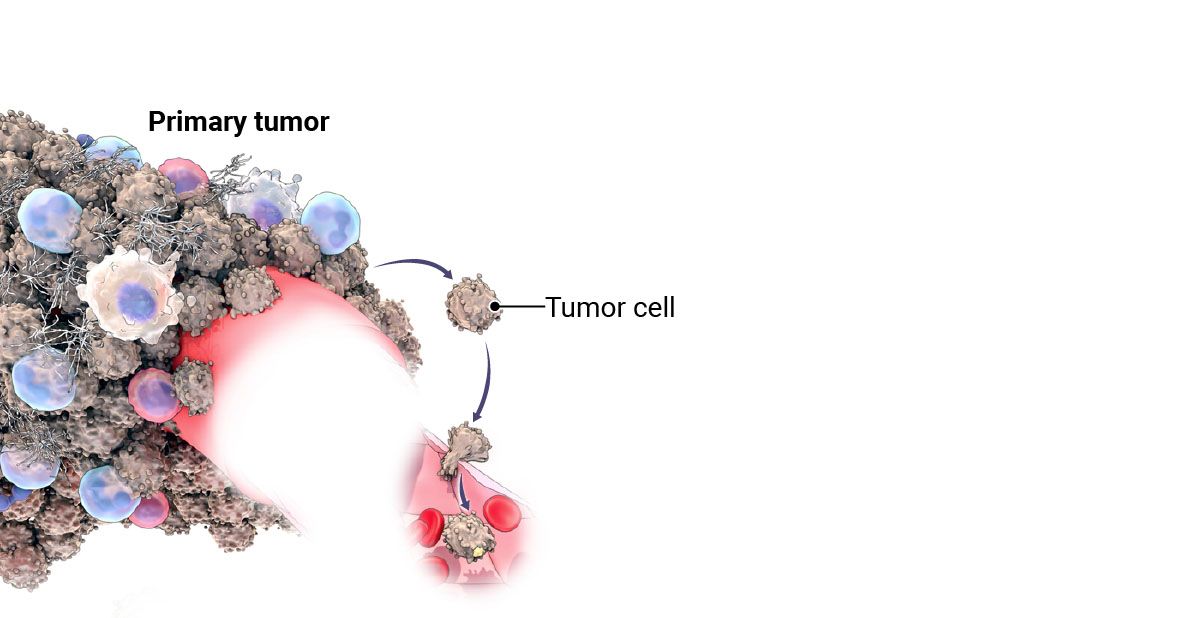
Una célula cancerosa se desprende lentamente del tumor original y comienza a infiltrarse en el tejido circundante. Al llegar a un vaso sanguíneo cercano, la célula errante atraviesa la pared externa y se deja llevar por la corriente como un kayakista que desciende rápidos. Tras recorrer el torrente sanguíneo durante unos segundos o minutos, la célula se retira en un lugar prometedor, sale del vaso y comienza a dividirse, estableciendo así un nuevo punto de anclaje para el cáncer.
Estas diseminaciones celulares suelen ser mortales para los pacientes. Hasta el 90% de las muertes por cáncer se deben a estas ramificaciones tumorales, conocidas como metástasis, y no al tumor original.
Pero la metástasis también es peligrosa para las células errantes. Como explica el biólogo especializado en cáncer Nicola Aceto, de la ETH Zúrich, el torrente sanguíneo es como «un río muy turbulento poblado de pirañas». Las probabilidades de que una célula tumoral sobreviva al viaje y prospere en otro lugar son minúsculas. Aun así, durante mucho tiempo se creyó que, a pesar de los riesgos, la mayoría de las células tumorales intentan el viaje solas.
De hecho, suelen hacerlo en grupo, formando cúmulos que pueden contener desde dos hasta más de 100 miembros y que a menudo incluyen células no tumorales (véase el gráfico a continuación). Durante la última década, Aceto y otros investigadores han documentado que el desplazamiento colectivo ofrece una gran ventaja a las células malignas.
“Los grupos de células cancerosas son mucho más eficaces para generar metástasis que las células cancerosas individuales”, afirma Andrew Ewald, biólogo especializado en células cancerosas de la Universidad Johns Hopkins.
En el cáncer de mama, por ejemplo, estudios en animales sugieren que los cúmulos, conocidos como células tumorales circulantes (CTC), tienen entre 50 y 100 veces más probabilidades de producir metástasis que las células aisladas. «Cuando encontramos estos cúmulos en la sangre, es un mal pronóstico», afirma el biólogo oncológico Kevin Cheung, del Centro Oncológico Fred Hutchinson
Según Aceto, PAGE Therapeutics, una empresa cofundada por él, ha estado desarrollando compuestos más eficaces para disolver los cúmulos y planea someterlos a un ensayo de seguridad. Los científicos también buscan otras maneras de dispersar los cúmulos o evitar su formación. «Hemos observado que los cúmulos de CTC están estrechamente relacionados con la supervivencia del paciente», afirma la bióloga especializada en cáncer Huiping Liu, de la Facultad de Medicina Feinberg de la Universidad Northwestern. Al manipular estos cúmulos, explica, los investigadores esperan brindar a los pacientes más tiempo de vida y mejorar su calidad de vida.
Hasta mil millones de células pueden desprenderse de un tumor primario cada día, y los científicos saben desde hace tiempo que a veces viajan juntas por el torrente sanguíneo. Por ejemplo, los patólogos que examinan muestras de tejido a veces encuentran cúmulos de células cancerosas, o émbolos tumorales, alojados en los capilares.
En 1953, el patólogo Satoru Watanabe, de la Facultad de Medicina de Yale, fue uno de los primeros en estudiar cómo los cúmulos celulares contribuyen a la metástasis. Inyectó a algunos ratones con cúmulos de células tumorales y a otros les administró células cancerosas separadas en una suspensión. Todos los animales que recibieron los cúmulos, excepto uno, desarrollaron metástasis pulmonares, mientras que ninguno de los ratones inyectados con células separadas las desarrolló. Estudios posteriores, que utilizaron métodos similares, también sugirieron que, al agruparse, las células mejoraban sus probabilidades de metastatizar. Sin embargo, la mayoría de los científicos pasaron por alto estos resultados y se centraron en las capacidades de las células aisladas.
El torrente sanguíneo es como un río muy turbulento poblado de pirañas.
- Nicola Aceto ETH Zúrich
Las nuevas formas de capturar y rastrear cúmulos celulares dificultaron su detección. A principios de la década de 2000, el biólogo especializado en cáncer Dan Haber y el ingeniero biomédico Mehmet Toner, ambos de la Facultad de Medicina de Harvard, junto con sus colegas, diseñaban chips microfluídicos, pequeños dispositivos con una red de canales finísimos. Los investigadores utilizaban estos chips para analizar muestras de sangre de pacientes y aislar células cancerosas individuales, lo que consideraban útil para el diagnóstico. Sin embargo, a veces, los dispositivos atrapaban cúmulos de células, recuerda Haber. Decidió entonces examinar más de cerca estas raras agregaciones. «No tenía ni idea de que resultaría tan fascinante», afirma.
Aceto estuvo a punto de perder la oportunidad de trabajar en ese estudio. Tras finalizar su doctorado, casi abandonó la investigación. Él y su esposa acababan de tener su primer hijo, y una carrera académica le parecía demasiado incierta. «Al final, seguí mi pasión» y comencé un posdoctorado en el laboratorio de Haber en 2012, recuerda. «En cuanto llegué, me di cuenta del potencial de los cúmulos de CTC y centré todo mi trabajo en ellos».
El primer desafío fue desarrollar una forma de etiquetar los cúmulos para que los investigadores pudieran rastrearlos y determinar si generaban metástasis. Aceto y sus colegas modificaron genéticamente células de tumores de mama humanos para que produjeran una proteína fluorescente verde o roja. Cuando se inyectó una mezcla bicolor de estas células en ratones, se generaron tumores que también eran una mezcla de ambos colores, al igual que casi todos los cúmulos que estos tumores desprendieron en el torrente sanguíneo.
Entonces Aceto y sus colegas realizaron la prueba de fuego: examinaron las metástasis de los pulmones de los animales bajo el microscopio. Si las masas provenían de células individuales, serían completamente verdes o completamente rojas. Pero si las metástasis crecían a partir de grupos de células que habían circulado juntas por el torrente sanguíneo, serían moteadas. «Vimos que las metástasis eran en su mayoría multicolores», recuerda Aceto. «Fue entonces cuando nos tomamos la primera cerveza para celebrar», dice.
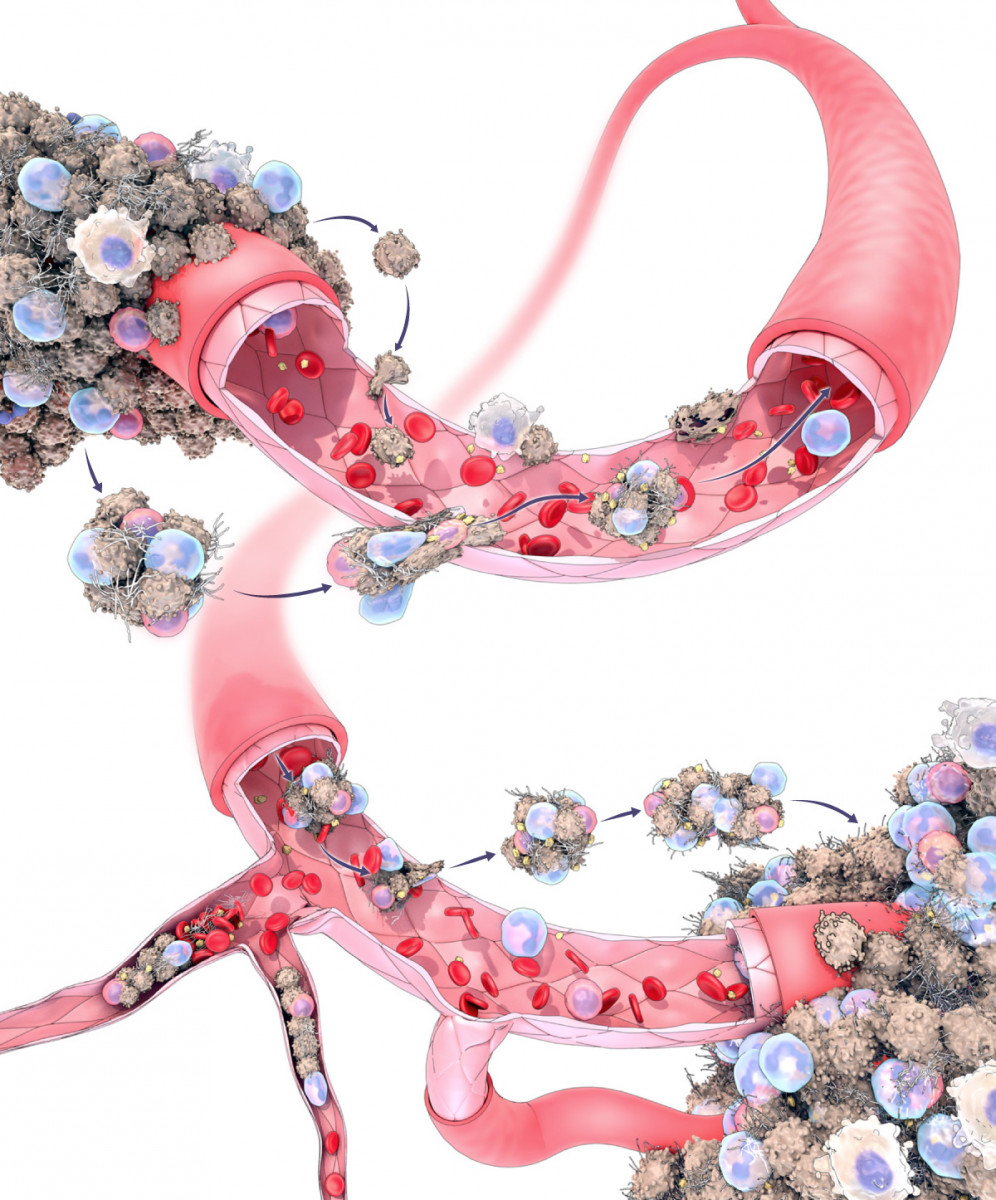
Bombas de racimo del cáncer
C. BICKEL/ Ciencia
Los resultados, publicados en Cellen 2014, y otros estudios contribuyeron a reevaluar los cúmulos celulares. Los investigadores siguen creyendo que muchas metástasis son causadas por células individuales. Sin embargo, Liu afirma que existen pruebas contundentes de que los cúmulos también desempeñan un papel importante. Además, los científicos han descubierto que diversos tipos de células pueden agruparse con las células tumorales y ayudarlas en su propagación, como las plaquetas, las células inmunitarias y los fibroblastos.
Además de los chips microfluídicos, los investigadores han recurrido a otras tecnologías para identificar cúmulos de CTC. CellSearch, una prueba comercial, utiliza anticuerpos sensibles a proteínas características del epitelio. Este tejido protector recubre muchas partes del cuerpo, como la piel, los intestinos, la boca y los pulmones, y es el origen de la mayoría de los cánceres. Mediante métodos como estos, los científicos han detectado cúmulos de células tumorales en pacientes con diversos tipos de cáncer, como el de mama, próstata, páncreas, colon y pulmón.
Pero estos cúmulos solo aparecieron en un subconjunto de pacientes y eran escasos. En la circulación de una persona con cáncer, puede haber una célula tumoral por cada 10 mil millones de células sanguíneas, y la mayoría de los estudios sugieren que estos cúmulos son aún más raros.
mil millones
Un tumor puede desprender células cada día.
~2–100
células en cada grupo canceroso
El ingeniero biomédico David Juncker, de la Universidad McGill, cree que estos hallazgos subestiman la verdadera abundancia de cúmulos. Él y sus colegas sospechaban que los métodos de detección, como los chips microfluídicos, son lo suficientemente agresivos como para fragmentar muchos cúmulos, distorsionando así las cifras. Los científicos idearon un enfoque diferente: llenar tubos verticales con sangre y dejar que gotee a través de filtros, un método de separación que, según Juncker, tiene menos probabilidades de fragmentar un cúmulo que bombear el fluido a través de un chip. Los 30 pacientes con cáncer analizados con este nuevo método presentaban cúmulos en la sangre, según revelaron él y sus colegas en 2025 en Communications Medicine .
En 10 de los pacientes, los cúmulos eran más frecuentes que las células tumorales individuales. «Si se actúa con menos delicadeza, aparecen más cúmulos y, en algunos pacientes, pueden constituir la mayoría» del cáncer circulante, afirma Juncker.
La presencia de cúmulos celulares en la sangre puede indicar la gravedad del cáncer, y el número de agregaciones aumenta a medida que la enfermedad progresa. Un estudio de 2025 publicado en Nature Medicine sugiere que estos cúmulos celulares también presagian la muerte, o incluso podrían promoverla mediante un mecanismo no relacionado con la metástasis. Un equipo liderado por Aceto y dos colegas del Centro Médico Southwestern de la Universidad de Texas, la médica de cuidados paliativos Kelley Newcomer y el biólogo oncológico y cirujano oncólogo Matteo Ligorio, midió los cúmulos circulantes en muestras de sangre de pacientes con cáncer terminal en cuidados paliativos. En los días previos al fallecimiento de los pacientes, el número de cúmulos aumentó considerablemente. Según Ligorio, no está claro si este aumento contribuyó directamente al fallecimiento de los pacientes o si reflejó otro proceso mortal.

Para las células cancerosas metastásicas, las células acompañantes facilitan el proceso. «Es como un decatlón», afirma Ewald. Al igual que los decatletas deben destacar en pruebas tan diversas como el salto de longitud, el lanzamiento de disco y el salto con pértiga, las células migratorias se enfrentan a desafíos dispares, como atravesar la matriz extracelular, entrar en los vasos sanguíneos y crecer en un nuevo entorno.
Viajar por el torrente sanguíneo puede ser el mayor desafío. Aunque las células metastásicas solo pasan un breve tiempo en circulación, durante ese periodo «no están a gusto», afirma Haber. Para empezar, la sangre que fluye por un vaso produce una fuerza de torsión que puede destrozar una célula cancerosa. Cuando se aíslan de sus congéneres, las células cancerosas suelen autodestruirse mediante un proceso llamado anoikis. Una célula tumoral solitaria también es presa fácil para las células inmunitarias, las pirañas que mencionó Aceto. En principio, unirse a un grupo debería proteger a una célula de estos tres peligros.
Sin embargo, los cúmulos no son simples masas de células adheridas entre sí con desesperación. Los investigadores han descubierto que las células cooperan y se adaptan. Pueden modificar su naturaleza para asemejarse más a las células madre, cuya capacidad de dividirse y diversificarse puede ayudarlas a arraigarse en un nuevo lugar. Incluso forman estructuras únicas que pueden aumentar sus probabilidades de supervivencia.
Por ejemplo, al estudiar los cúmulos celulares desprendidos de melanomas en el pez cebra, el biólogo celular y oncólogo Richard White, de la Universidad de Oxford, y sus colegas descubrieron que las células suelen adoptar una disposición específica. Los tumores pueden contener dos subtipos de células: una variedad especialmente eficaz para invadir tejidos y otra con gran capacidad de proliferación. En los cúmulos, las células invasoras generalmente se ubican en la periferia, mientras que las proliferativas se asientan en el interior. Esta organización, descrita en 2021 en la revista Developmental Cell , podría ser ventajosa, según White, porque las células invasoras podrían proteger a sus compañeras del sistema inmunitario.
Los cúmulos de células tumorales circulantes están estrechamente relacionados con la supervivencia del paciente.
- Huiping Liu Universidad Northwestern
Haber, Toner y sus colegas descubrieron que las células no necesariamente permanecen fijas en su posición. Los cúmulos pueden cambiar de forma al encontrar obstáculos. Muchos de los glóbulos celulares son lo suficientemente grandes como para quedar atrapados en los capilares. Sin embargo, a veces logran atravesar los vasos de pequeño diámetro. Para averiguar cómo, los científicos obligaron a los cúmulos a cruzar un chip microfluídico con canales estrechos. Para su sorpresa, las esferas de células se alargaron formando cadenas que podían deslizarse por los conductos en fila india. Posteriormente, recuperaron su forma original, según informaron los científicos en un artículo de 2016 publicado en las Actas de la Academia Nacional de Ciencias ( PNAS ). «Salen con forma de salchicha y, en cuestión de segundos, se reorganizan en un cúmulo», explica Haber.
Hasta ahora, ningún tratamiento contra el cáncer bloquea específicamente la metástasis. Sin embargo, los descubrimientos sobre cómo se forman y funcionan los cúmulos de células tumorales circulantes (CTC) sugieren varias maneras de prevenir la propagación del cáncer. Aceto y sus colegas han sido quienes más han avanzado. Probaron cerca de 2500 fármacos aprobados para determinar si podían desintegrar los cúmulos en un cultivo celular. Dos de los más eficaces bloquean la bomba de sodio-potasio, una proteína que intercambia estos dos iones a través de la membrana celular. Este hallazgo tenía sentido, ya que estudios previos habían sugerido que la inhibición de la bomba debilita las conexiones entre las células.
Para evaluar si este mecanismo funciona en el organismo, Aceto y su equipo iniciaron en 2020 el ensayo de fase 1 de digoxina, un fármaco para la insuficiencia cardíaca que inhibe la bomba de sodio-potasio, en pacientes con cáncer de mama. Los investigadores extrajeron sangre de las pacientes, les administraron digoxina durante 7 días y luego tomaron más muestras de sangre. Los cúmulos en la sangre de las pacientes se redujeron en aproximadamente dos células durante esa semana. El primer ensayo de seguridad de PAGE Therapeutics con un compuesto más potente para disolver los cúmulos podría comenzar el próximo año, según Aceto.
Otra posible forma de separar los cúmulos proviene de la ingeniera biomédica Anne-Laure Papa de la Universidad George Washington y sus colaboradores. A medida que los conglomerados se desplazan por el sistema circulatorio, pueden acumular la proteína fibrina, un componente filamentoso de los coágulos sanguíneos que une las células cancerosas. Los fragmentos celulares formadores de coágulos, conocidos como plaquetas, suelen recubrir los cúmulos. En una serie de experimentos, los científicos crearon lo que denominaron «señuelos de plaquetas» sumergiendo los fragmentos celulares en detergente, lo que impide que formen coágulos. Posteriormente, los investigadores impregnaron los señuelos con tPA, un fármaco trombolítico utilizado para tratar infartos y accidentes cerebrovasculares que disuelve la fibrina, y los inyectaron en ratones que también habían recibido inyecciones de cúmulos de células tumorales.
En comparación con los animales que recibieron solo tPA, los ratones tratados con los señuelos de plaquetas desarrollaron metástasis más pequeñas y sobrevivieron aproximadamente un 10 % más, según informaron los investigadores en 2024 en Advanced Healthcare Materials . «Será necesario realizar trabajo adicional antes de un ensayo clínico», afirma Papa, como por ejemplo, ajustar «la dosis y el esquema de inyección».
Dispersar los cúmulos de células tumorales podría no ser suficiente. «La pregunta que queda es: si los desintegramos, ¿cuánto se reduce el potencial metastásico?», dice Cheung. Liu cree que se necesitará una estrategia multifacética para combatir los cúmulos. «Ojalá fuera tan sencillo como para que existiera una solución mágica. La realidad es que es complejo». Los investigadores probablemente tendrán que atacar los cúmulos con varios fármacos, incluidos compuestos que aumentan su vulnerabilidad al sistema inmunitario, añade.
Su laboratorio descubrió que los cúmulos tumorales que circulan en pacientes con cáncer de mama suelen albergar un tipo raro de célula inmunitaria centinela conocida como célula T doble positiva. Estas células, que poseen los receptores CD4 y CD8, representan menos del 0,1 % de las células T en la sangre, pero constituyen más del 14 % de las células inmunitarias en los cúmulos de CTC de las pacientes, según revelaron los científicos en 2025 en el Journal of Clinical Investigation . La presencia de estas células aumentó las probabilidades de que un cúmulo metastatizara en ratones. Además, el análisis del equipo de Liu sugirió que estas células ayudan a suprimir los ataques inmunitarios contra los cúmulos.
Para unirse a un grupo, según revelaron los investigadores, una célula T doble positiva requiere otro receptor en su superficie, VLA-4, que se conecta a una proteína correspondiente en una célula tumoral. Liu y sus colegas determinaron que administrar a ratones con tumores implantados un anticuerpo que bloquea VLA-4 redujo la metástasis y duplicó con creces las probabilidades de que los animales sobrevivieran al menos 6 semanas. Una versión humana del anticuerpo, natalizumab, ya ha sido aprobada para el tratamiento de la esclerosis múltiple y la enfermedad de Crohn. Liu afirma que ella y su equipo están intentando organizar un ensayo clínico del fármaco en pacientes con cáncer de mama. También están desarrollando un compuesto para bloquear una proteína diferente que protege a los grupos del sistema inmunitario.
Según Cheung, la mejor manera de frenar la metástasis podría ser impedir la formación de cúmulos desde el principio. Cuando los cánceres alcanzan cierto tamaño, suelen sufrir necrosis, un proceso en el que muere el interior de la masa tumoral. Cheung y sus colegas informaron en 2023 en PNAS que el número de cúmulos en la sangre de ratas se multiplicó por diez cuando se produjo la necrosis . Sin embargo, cuando los investigadores implantaron tumores que carecían de una proteína clave necesaria para la necrosis en los animales, los cúmulos prácticamente desaparecieron. «Hemos descubierto que si se previene la necrosis, se reducen las CTC y los cúmulos de CTC a cero», afirma Cheung. Su laboratorio está intentando ahora crear un anticuerpo que actúe sobre la proteína e inhiba la necrosis.
Para una célula cancerosa, pertenecer a un grupo no garantiza que encuentre un nuevo hogar. Sin embargo, viajar en grupos parece otorgar a las células errantes la ventaja suficiente para que algunas completen su marcha hacia la muerte. Los investigadores del cáncer ahora esperan inclinar la balanza en contra de las células cancerosas y a favor de los pacientes.


