Conseguir hidrógeno a partir del aire ya es posible
- Toyota Motor Europe (TME) y DIFFER, el Instituto holandés de investigación energética fundamental, se unen para desarrollar un dispositivo que permite obtener hidrógeno a partir del aire.
- La producción de hidrógeno a partir de fuentes de energía renovables permite reducir las emisiones de gases de efecto invernadero.

Parece cosa de magia: basta con poner un dispositivo especial en contacto con el aire y exponerlo a la luz del sol y empieza a producir combustible, sin ningún coste. Esa es la idea básica que subyace a la importante investigación llevada a cabo por DIFFER, el Instituto holandés de investigación energética fundamental, en colaboración con Toyota Motor Europe (TME). El objetivo de dicha alianza es desarrollar un dispositivo que absorba el vapor de agua y lo separe directamente en hidrógeno y oxígeno usando la energía del sol.
Objetivos comunes
En este proyecto, DIFFER y TME exploran una forma innovadora de producir hidrógeno directamente a partir de aire húmedo. Esta investigación tiene dos objetivos distintos. Por un lado, se necesitan nuevos combustibles sostenibles para disminuir nuestra dependencia de los combustibles fósiles y, por otro, es necesario reducir las emisiones de gases de efecto invernadero. Uno de esos combustibles sostenibles es el hidrógeno, que se puede utilizar para almacenar energía renovable. Cuando el hidrógeno se combina con oxígeno en una pila de combustible, la energía se libera en forma de electricidad, emitiendo como único residuo vapor de agua.
En su búsqueda respectiva de soluciones, la división de Investigación Avanzada de Materiales de TME se ha unido al grupo de Procesos Catalíticos y Electroquímicos para Aplicaciones Energéticas de DIFFER, encabezado por Mihalis Tsampas. Este grupo había estado trabajando en un método para separar el agua en estado gaseoso en lugar de en estado líquido, que es mucho más común. “Trabajar con gas en lugar de con líquido tiene varias ventajas”, explica Tsampas.
“Los líquidos presentan ciertos problemas técnicos, como la formación no deseada de burbujas. Además, al utilizar agua en estado gaseoso y no en estado líquido, no necesitamos instalaciones costosas para purificar el agua. Y, por último, puesto que solo utilizamos el agua presente en el aire que nos rodea, nuestra tecnologías también es aplicable a lugares remotos donde no hay agua disponible”.

segunda versión de su camión de pila de combustible cero emisiones
Principio demostrado
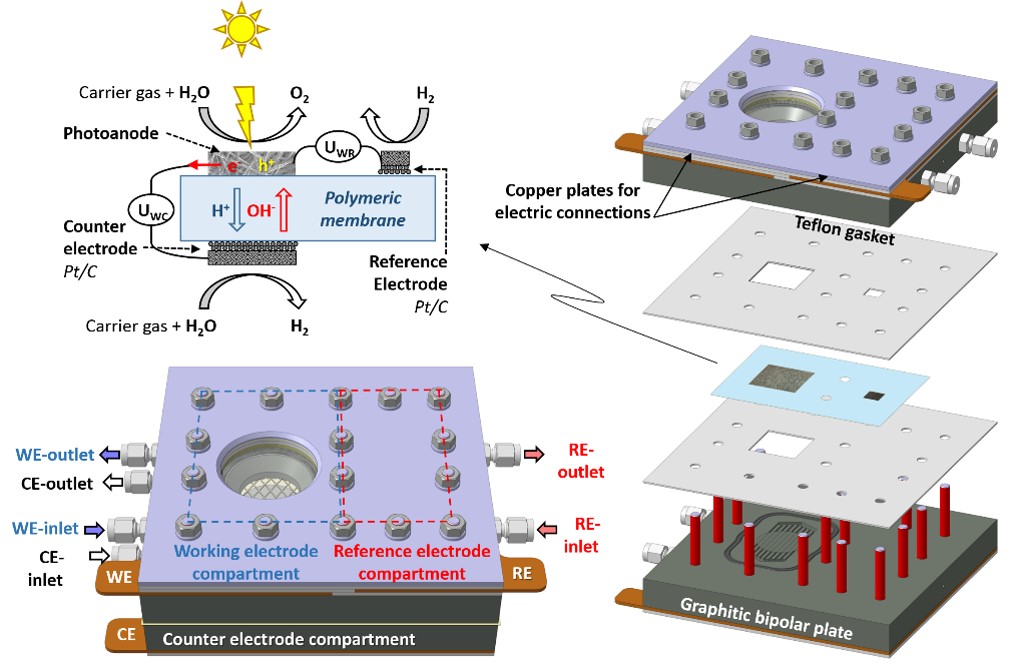
A lo largo del pasado año, DIFFER y TME han demostrado en un estudio conjunto de viabilidad que el principio planteado realmente se cumple. Los investigadores han desarrollado una nueva célula fotoelectroquímica de estado sólido que por primera vez puede obtener agua del aire y luego generar hidrógeno a partir de la iluminación con luz solar. Este primer prototipo alcanzó un impresionante 70% del rendimiento que se obtiene al llenar un dispositivo equivalente con agua. El sistema consta de unas membranas de electrolitos poliméricos, unos fotoelectrodos porosos y unos materiales que absorben el agua, combinados en un dispositivo de diseño especial integrado en la membrana.
El enfoque de Toyota
“Además de desarrollar la primera berlina del mundo a base de hidrógeno fabricada en serie, Toyota contribuye activamente a buscar formas de producir hidrógeno sin recurrir a combustibles fósiles”, ha declarado Isotta Cerri, directora general de Investigación avanzada de materiales. “Esto encaja con los retos del Desafío medioambiental de Toyota 2050, que aspira a eliminar las emisiones de CO2 durante todo el ciclo de vida de nuestros vehículos. La producción de hidrógeno a partir de fuentes de energía renovables ayuda sustancialmente a reducir las emisiones de gases de efecto invernadero. Con este tipo de investigación fundamental, trabajamos con el objetivo de conseguir una sociedad basada en el hidrógeno mediante el desarrollo de aplicaciones del hidrógeno asequibles y fáciles de usar, tanto para nuestras operaciones como para los clientes”.

primera embarcación de hidrógeno del mundo
Mejoras y ampliación de la escala
En la siguiente fase del proyecto, los colaboradores se proponen mejorar considerablemente el proceso. “En nuestro primer prototipo, utilizamos fotoelectrodos que se sabe que son muy estables. Sin embargo, el material empleado solo absorbe la luz ultravioleta, que supone menos del cinco por ciento de toda la luz solar que llega a la Tierra”, explica Tsampas, quien añade: “El siguiente paso, por tanto, es aplicar materiales de vanguardia y optimizar la estructura del sistema para incrementar tanto la entrada de agua como la cantidad de luz solar que se absorbe”.

tecnología de hidrógeno en Europa a Caetanobus SA (Portugal)
Una vez superado ese obstáculo, las labores de investigación se centrarán en ampliar la escala de la tecnología. Las células fotoelectroquímicas capaces de producir hidrógeno son muy pequeñas, alrededor de un centímetro cuadrado. Para que sean económicamente viables, su tamaño debe aumentar en al menos dos o tres órdenes de magnitud.
“Aún no estamos en ese nivel, pero esperamos que algún día ese tipo de sistemas se puedan llegar a utilizar como fuente de energía en las viviendas particulares o en el repostaje de los vehículos para realizar desplazamientos cotidianos», pronostica Tsampas.
El proyecto de investigación LIFT –Launchpad for Innovative Future Technology o Plataforma de Lanzamiento de Tecnologías Innovadoras de Futuro– ha obtenido una subvención de la fundación ENW PPS de la Organización Neerlandesa para la Investigación Científica (NWO).
PROCESOS CATALÍTICOS Y ELECTROQUÍMICOS PARA APLICACIONES ENERGÉTICAS.
LÍDER DEL GRUPO: DR. MIHALIS TSAMPAS.
Las fuentes de energía renovable son altamente deseables en esta era de la disminución de las reservas de petróleo y el aumento de las preocupaciones ambientales. La energía solar y la energía eólica pueden cubrir una parte sustancial de las necesidades energéticas mundiales, pero debido a la intermitencia y la dilución de estas fuentes, se requiere el almacenamiento en productos de alta densidad energética. En el grupo de procesos catalíticos y electroquímicos para aplicaciones de energía, combinamos la electroquímica de estado sólido con (foto) catálisis y química de plasma para mejorar la eficiencia de los existentes y desarrollar nuevas rutas para el almacenamiento de energía.
Nuestras actividades se dividen en tres categorías principales:
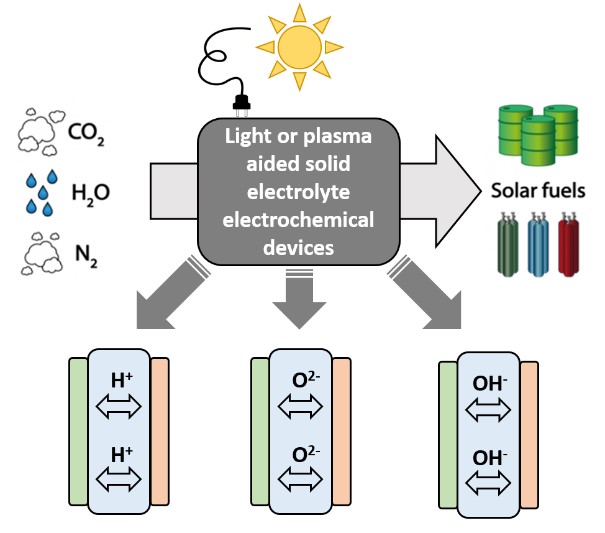
- Conductores iónicos poliméricos para electrólisis / electrosíntesis foto asistida por debajo de 200 o C. Llevamos a cabo investigaciones sobre el desarrollo de materiales nanoestructurados para ser utilizados como fotoanodos o fotocátodos junto con membranas de electrolitos poliméricos y soportes de alta superficie. Para evaluar la actividad de nuestros fotoelectrodos, hemos desarrollado un nuevo diseño de reactor que funciona con reactivos gaseosos y está equipado con un electrodo de referencia confiable. Los ensamblajes de membrana y fotoelectrodo ofrecen modos de operación novedosos en comparación con las células fotoelectroquímicas convencionales. Por ejemplo, aparte de síntesis electrocombustibles photoassisted a través de la electrólisis del agua y CO 2 La hidrogenación, la generación de hidrógeno se puede lograr a partir de la humedad del aire ambiente creando un proceso «neutral en agua».
- Conductores de iones de oxígeno de cerámica o de protones para la electrólisis / electrosíntesis por encima de 400 o C. Nosotros llevamos a cabo investigaciones sobre (i) nuevos perovskitas para eficiente y estable CO 2 / H 2 O co-electrólisis hacia gas de síntesis con CO / H controlados 2 proporciones (en colaboración con Syngaschem BV) y (ii) combinación de excitación vibracional y electrocatálisis para la valorización de CO 2 / H 2 O (en colaboración con UTwente y Shell) y la producción de amoníaco plasmo-electroquímico. Estos reactores también se implementan para la promoción electroquímica de reacciones catalíticas.
- Baterías de azufre y sodio. En colaboración con Exergy Storage, nuestro objetivo es realizar un prototipo de batería de sodio-azufre (NaS) basada en alúmina de ion sodio que funcione en una ventana de temperatura intermedia (150-200 o C) adecuada para la unidad de almacenamiento residencial. Nos centramos en los desafíos relacionados con el compartimiento catódico de NaSBs.
INVESTIGACIÓN
CELULAS FOTOELECTROQUÍMICAS PARA COMBUSTIBLES SOLARES
Una celda PEC es un dispositivo que potencialmente puede lograr la división del agua y, por lo tanto, la producción de hidrógeno o la conversión de CO 2 en combustible, utilizando la luz solar como la única entrada de energía. La mayoría de las células PEC descritas hasta ahora en la literatura están diseñadas para operar en fases líquidas. Las principales desventajas de estas células es la baja solubilidad del CO 2 en medios líquidos y la dificultad para escalar.
En nuestro grupo, nos centramos en la optimización de un diseño alternativo de reactor y electrodo PEC que pueda superar estas dificultades mediante la operación en fase gaseosa. El diseño del reactor está inspirado en electrolizadores de membrana de electrolito polimérico (PEM) y, por lo tanto, los dos electrodos de PEC se separan con una membrana polimérica iónicamente conductora. Estas células PEM-PEC ofrecen una variedad de ventajas en comparación con el PEC líquido convencional, ya que permiten la operación en fase gaseosa, lo que garantiza un fácil acceso de CO 2 al electrodo, la separación directa de los productos de reacción y también ofrece la posibilidad de capturar agua del aire ambiente. (lo que implica que virtualmente no se necesita agua líquida para la operación, lo que lo convierte en un proceso sin agua).
Nuestros fotoelectrodos generalmente son compatibles con una red de Ti de microfibras. Los electrodos convencionales de capa de difusión de gas ( nanopartículas de TiO 2 decoradas con microfibras de carbono) sufren una fuerte recombinación de los pares de orificios de electrones en los límites de las partículas de TiO 2 y una estabilidad térmica deficiente del sustrato de carbono. Para resolver estos inconvenientes, hemos desarrollado y utilizado con éxito los fotoanodos de matrices de nanotubos de titanio, preparados por anodización electroquímica de una red de Ti y su posterior recocido con oxígeno. La carga de los sustratos con poca cantidad de Pt mediante la Deposición de Capa Atómica (colaboración con el grupo PMP de TU / e) está en progreso.
Como segundo paso y para adaptar nuestro concepto a la parte visible del espectro solar (TiO 2 se limita a la irradiación con luz UV), sintetizamos una nueva clase de fotoanodos utilizando la heterounión WO3 / BiVO4 sobre sustratos de titanio porosos. Esto se logró en colaboración con el grupo FNA de TU / e mediante la combinación de la anodización electroquímica de las capas de tungsteno pulverizadas y la formación de BiVO 4 mediante el método SILAR (Sucesión y reacción de la capa iónica sucesiva). Usando estos fotoanodos, logramos por primera vez la división en agua en fase gaseosa con rendimientos similares a los de las células fotoelectroquímicas de electrolito líquido convencionales bajo irradiación de luz visible y sin el uso de un co-catalizador.
La investigación en curso se centra en el posible uso de membranas de intercambio de iones de hidróxido (colaboraciones con la Universidad de Newcastle y con la Academia de Ciencias de Bulgaria) para obtener un entorno alcalino que debería aumentar la eficiencia del sistema. Dentro de esta perspectiva, también se consideran modificaciones adicionales de los electrodos, como la adición de capas protectoras de óxidos (es decir, TiO 2 , SnO) y / o cocatalizadores (por ejemplo, CoO x , Ni-Fe-OOH) para garantizar una mayor estabilidad y actuaciones Finalmente, se utilizan fotocátodos basados en nanorods de Cu 2 O para la valorización de CO 2 / H 2 O en la célula PEM-PEC.
CÉLULAS ELECTROLITAS DE ÓXIDO SÓLIDO PARA COMBUSTIBLES SOLARES
El gas de síntesis, el monóxido de carbono y el hidrógeno es un intermediario clave para las reacciones que producen químicos ricos en energía, como el gas natural sintético (SNG) y los combustibles líquidos (a través de la síntesis de Fischer-Tropsch). Estos productos químicos son fáciles de usar y almacenar y son compatibles con la infraestructura existente. Son especialmente importantes para almacenar el exceso de electricidad inherente a las fuentes de energía intermitentes, como la energía solar y eólica.
CONDUCTORES DE IONES DE OXÍGENO
En cooperación con Syngaschem, investigamos la coelectrólisis del agua a alta temperatura y el dióxido de carbono a gas de síntesis utilizando conductores de iones de oxígeno. La alta temperatura (co) electrólisis es el proceso inverso de la operación de la celda de combustible y, por lo tanto, se utilizan materiales similares. Los materiales más modernos para una celda de combustible de óxido sólido (SOFC), son circonia estabilizada con itria (YSZ) para el electrólito, materiales compuestos de Ni / YSZ, cermet, para el electrodo de combustible y La 0.85 Sr 0.15 MnO 3 ± δ (LSM) o La 0.6 Sr 0.4 Co 0.2 Fe 0.8 O 3 ±(LSCF) perovskites en combinación con YSZ o GDC (ceria dopada con gadolinio) para el electrodo de oxígeno. Ni / YSZ muestra excelentes propiedades catalíticas para la oxidación del combustible y una buena recolección de corriente, sin embargo, presenta desventajas, como la deposición de carbono y un ciclo de redox deficiente que causa inestabilidad en el volumen. En el caso de las aplicaciones de (co) electrólisis, el Ni se oxida, lo que conduce a un electrodo de NiO / YSZ que no posee la importante funcionalidad de la recolección de corriente (NiO es un conductor deficiente). Por lo tanto, Ni / YSZ no se puede usar directamente en aplicaciones de (co) electrólisis (solo es posible si hay co-alimentación de H 2 que conserva el níquel en su forma metálica).
La investigación de electrólisis actual se dirige principalmente al descubrimiento de un material de electrodo de combustible alternativo basado principalmente en perovskitas estables redox (mientras se implementan los electrodos de oxígeno SOFC). Un enfoque atractivo para el diseño de materiales de perovskita con soporte de nanopartículas es el crecimiento in situ de nanopartículas metálicas de la perovskita original (exsolución). Las nanopartículas eliminadas se encajan en la superficie de la perovskita, lo que evita la aglomeración y el engrosamiento de las nanopartículas durante las condiciones de operación y, por lo tanto, ofrece una nueva clase de materiales de electrodos activos. Nuestro objetivo es mejorar el rendimiento del material del electrodo de combustible basado en la solución de metales de transición de las perovskitas (junto con la Universidad de Newcastle) tomando información de la química computacional y las herramientas avanzadas de caracterización.
CONDUCTORES DE PROTONES
Nuestro objetivo es desarrollar un electrolizador de óxido sólido conductor de protones para la síntesis directa de hidrocarburos y / o alcoholes a partir de CO 2 y H 2 O. En el sistema propuesto H 2 O se oxida en el ánodo, mientras que el CO 2 es in situ reducida en condiciones de carga y en presencia de un electrocatalizador apropiado para hidrocarburos y / o alcoholes (por ejemplo, CH 4 , CH 3OH) Promover la selectividad hacia este último. Para superar las posibles limitaciones de la selectividad del producto y mejorar la cinética de la reacción, se emplea la operación de la celda electroquímica con nuevas formulaciones de electrodos / electrolitos. Para una mayor adaptación de la selectividad del producto, el enfoque se combina con la estimulación vibratoria directa del CO adsorbido en el catalizador metálico, así como con la excitación vibratoria de las moléculas de COx (x = 1,2) presentes en la fase gaseosa adyacente al electrodo.
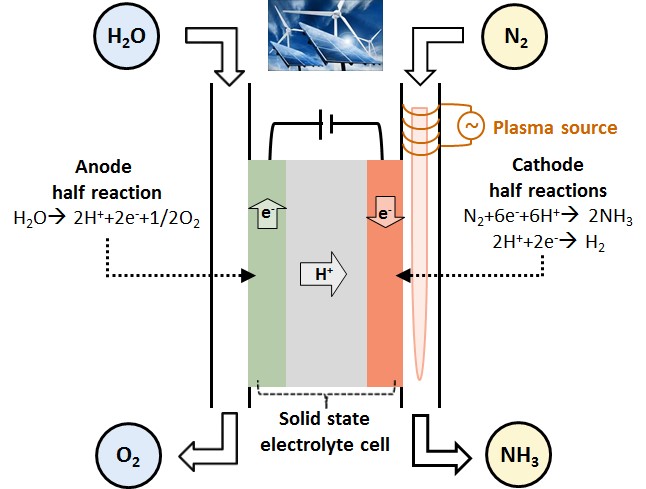
Sobre la base de conductores de protones, estamos desarrollando una tecnología totalmente eléctrica de reactor único que combina las fortalezas de la electrocatálisis y la activación por plasma en la conversión de energía renovable. El objetivo es mejorar la cinética de la reacción y / o la selectividad de las reacciones electroquímicas ascendentes (como la fijación de N 2).por agua), a través de la excitación por plasma de las moléculas. La siguiente figura ilustra el caso de un dispositivo electroquímico asistido por plasma para la síntesis de amoníaco a partir de agua y nitrógeno. El enfoque electroquímico convencional tiene una baja selectividad para la producción de amoníaco frente a la reacción de evolución de hidrógeno no deseada. Se ha identificado que la tasa de este proceso debe mejorarse en un factor de 50 para que sea comercialmente viable. El papel del plasma en nuestro enfoque es activar el nitrógeno y cambiar la selectividad hacia la síntesis de amoníaco incluso a densidades de corriente más altas y así mejorar la tasa de producción general a niveles comercialmente viables.
Los catalizadores industriales de síntesis de amoniaco (Fe, Ru) deben ser eficientes tanto en la disociación de N 2 como en la hidrogenación de los átomos de nitrógeno. En nuestro enfoque, estos dos pasos están separados y, por lo tanto, los catalizadores de hidrogenación (por ejemplo, materiales basados en Ni, Co) se explorarán como materiales candidatos. Además, se utilizará una membrana conductora de protones que opera a bajas temperaturas (por ejemplo, electrolito polimérico basado en Nafion o PBI) o intermedias (por ejemplo, electrolito cerámico BZY) para extender la ventana de temperatura de operación para la síntesis de amoníaco.
PROMOCIÓN ELECTROQUÍMICA DE LA CATÁLISIS.
El fenómeno del efecto de la promoción electroquímica de la catálisis (EPOC) se refiere a los cambios pronunciados, reversibles y controlados en las propiedades catalíticas (actividad y selectividad) en la polarización eléctrica. En los estudios de EPOC, se emplean células electroquímicas, en las que uno de los electrodos es el catalizador para la reacción en estudio. Al controlar la polarización, los iones pueden ser bombeados hacia o desde el catalizador, cambiando su función de trabajo y por lo tanto sus propiedades catalíticas. A pesar de las ventajas aparentes de este sistema, como el control in situ de la cobertura de los iones promotores, el EPOC aún no se ha aplicado en la industria, principalmente debido a la actividad mucho menor por masa catalítica que los polvos clásicos nanodispersos.
BATERIAS DE AZUFRE DE SODIO
Las baterías de sulfuro de sodio (NaSB) se consideran como sistemas de almacenamiento de energía potencial para aplicaciones de almacenamiento eléctrico estacionario. Las principales ventajas de los NaSB son la alta densidad de energía, la alta eficiencia de carga / descarga, el ciclo de vida prolongado y su fabricación a partir de materiales abundantes y de bajo costo. Las baterías NaSBs emplean sodio (Na) y azufre (S) como materiales de electrodos activos, y las membranas cerámicas de beta-alúmina (Al 2 O 3 ) como el electrolito conductor de Na +. Los NaSB tradicionales operan a altas temperaturas de 300-350 oC, donde ambos electrodos están en un estado fundido para tener la reactividad electroquímica óptima, y para que las membranas de beta-alúmina tengan la conductividad iónica óptima. Sin embargo, los problemas de seguridad relacionados con la operación a alta temperatura activaron nuevos conceptos de baterías NaSB, que apuntan a temperaturas de operación justo por encima del punto de fusión del sodio (es decir, 120-150 o C). Estas condiciones operativas presentan desafíos que deben abordarse para optimizar los nuevos NaSB. En este contexto, nos centramos en los desafíos relacionados con el compartimento catódico de NaSB. Investigamos el efecto de la composición del catolito y el refresco en la eficiencia y la estabilidad durante los ciclos de carga y descarga.
Acerca de DIFFER
DIFFER es el Instituto holandés de investigación energética fundamental, y uno de las nueve instituciones que componen la Organización neerlandesa para la investigación científica (NWO). El instituto lleva a cabo labores de investigación interdisciplinares en materiales, procesos y sistemas relacionados con una infraestructura global de energía sostenible, en estrecha colaboración con instituciones académicas e industriales nacionales e internacionales. La investigación de DIFFER cubre tanto la conversión como el almacenamiento de energía sostenible en combustibles solares, y la generación de una energía limpia, segura y abundante a través de la fusión nuclear.