Algunos gliomas adquieren resistencia a la quimioterapia
Madrid, agosto de 2020
Un equipo del CNIO y de la Universidad de Ciencia y Tecnología de Hong Kong identifica cómo algunos gliomas adquieren resistencia a la quimioterapia
- Los pacientes de gliomas –uno de los tipos más comunes de tumor cerebral– ven aumentada su supervivencia gracias al tratamiento combinado de radioterapia con temozolomida
- Los investigadores han descubierto un nuevo mecanismo por el que los tumores evaden la quimioterapia, mediante reordenamiento genómico del gen de reparación del ADN MGMT
- El hallazgo tiene potencial relevancia para actualizar los métodos con los que se monitoriza la eficacia de la temozolomida. Los reordenamientos genómicos podrían constituir un marcador que, mediante un análisis de sangre, ayudaría a tomar decisiones sobre los tratamientos
Un equipo liderado por Massimo Squatrito, jefe del Grupo de Tumores Cerebrales Fundación Seve Ballesteros del Centro Nacional de Investigaciones Oncológicas (CNIO), ha realizado un importante avance en la comprensión de cómo algunos gliomas pueden generar resistencia a la quimioterapia.
Massimo-Squatrito
Coordinado en colaboración con el laboratorio de Jiguang Wang, de la Universidad de Ciencia y Tecnología de Hong Kong, y Tao Jiang, del Instituto Neurológico de Beijing (China), el estudio proporciona nuevas pistas sobre cómo monitorizar la eficacia de las terapias. El trabajo se publica en Nature Communications. Algunos gliomas adquieren resistencia a la quimioterapia
A día de hoy, el principal y casi único tratamiento para los gliomas –uno de los tipos más comunes de tumor cerebral– es la combinación de radioterapia con el agente de quimioterapia llamado temozolomida, una estrategia que puede ampliar hasta un 30% la supervivencia de estos pacientes. Como la mayoría de la quimioterapia, la temozolomida induce daños en el ADN de las células tumorales. Los gliomas pueden progresar reparando este daño a través de una enzima codificada por el gen MGMT. En pacientes cuya actividad de MGMT está bloqueada a causa de una modificación de su promotor llamada ‘hipermetilación’, las células del cáncer no pueden reparar el daño producido por la temozolomida y colapsan.
Desafortunadamente, en torno a un 40-50% de los pacientes son resistentes a la temozolomida. Estos pacientes expresan altos niveles de MGMT y el tumor continúa creciendo aun bajo el tratamiento. Ahora, el estudio del CNIO y la Universidad de Ciencia y Tecnología de Hong Kong ha desvelado que un subtipo de pacientes adquiere una alteración genética específica que pueden evadir la terapia combinada.
El control cambia de manos
“Observamos que en un grupo de pacientes se producía una traslocación de MGMT”, explica Massimo Squatrito. “Estos reordenamientos genómicos involucran la fusión de MGMT con otros genes, lo que implica que MGMT pasa a estar regulado por los promotores con los que se ha funcionado, lo que contribuye a su sobreexpresión. Cuando se producen estos reordenamientos, el daño al ADN inducido por la temozolomida se repara y el glioma continúa creciendo incluso a pesar del tratamiento”.
El equipo de la Universidad de Ciencia y Tecnología de Hong Kong validó la presencia de estos reordenamientos en un subtipo de una gran cohorte de tumores recurrentes procedente de diferentes hospitales, principalmente del Hospital Beijing Tiantan. Utilizando la técnica de edición genómica CRISPR-Cas9, el equipo del CNIO replicó algunas de estas translocaciones en diferentes modelos animales y celulares y confirmó que pueden conferir resistencia a la temozolomida. “Parece que las translocaciones no están presentes en el tumor original, solo en los recurrentes, aquellos que surgen después de que el cáncer original se trate”, continúa Squatrito. “Esto indica que la resistencia puede ocurrir a consecuencia del propio tratamiento”. Algunos gliomas adquieren resistencia a la quimioterapia
El hallazgo puede llevar a cambios en los métodos con los que se monitoriza la eficacia de la terapia: “A día de hoy, el único marcador terapéutico conocido en gliomas es el análisis del estado del promotor de MGMT. Si está metilado, se silencia el gen MGMT y se predice que el paciente responderá a la temozolomida. Nuestro estudio demuestra que este método ya no has válido cuando se ha producido translocación genómica. Aunque su promotor siga bloqueado, el gen está siendo sobreactivado por otros promotores y contribuirá a la recurrencia del tumor”.
Otro importante resultado del trabajo en los modelos animales es que los investigadores han detectado la presencia de esta traslocación de MGMT en los exosomas, es decir, en las partículas que el glioma libera al torrente sanguíneo. “Si este hallazgo se confirma en pacientes, podría constituir una herramienta de detección temprana de resistencia. Mediante un sencillo análisis de biopsia líquida con solo unas muestras de sangre, podríamos saber qué pacientes están desarrollando resistencia a la temozolomida y ayudará a cambiar a otras opciones terapéuticas, cuando estén disponibles”.
En próximos pasos de la investigación, el equipo identificará nuevas formas de tratamiento para los pacientes resistentes a la temozolomida. Algunos gliomas adquieren resistencia a la quimioterapia
El trabajo ha sido financiado por el Instituto de Salud Carlos III, la Fundación Seve Ballesteros, la Asociación Española Contra el Cáncer (AECC), la Natural Science Foundation of China, el Research Grants Council de Hong Kong, la Beijing Municipal Administration of Hospitals, el Beijing Nova Program y la Beijing Talents Foundation.
Sobre la Universidad de Ciencia y Tecnología de Hong Kong
La Universidad de Ciencia y Tecnología de Hong Kong (HKUST) (www.ust.hk) es una universidad de investigación intensiva de clase mundial enfocada en ciencia, tecnología y negocios, así como humanidades y ciencias sociales. La HKUST ofrece un campus internacional y una pedagogía holística e interdisciplinaria para nutrir a sus graduados con una visión global, un fuerte espíritu emprendedor y un pensamiento innovador. La HKUST obtuvo la mayor proporción de trabajo de investigación excelente a nivel internacional en el Ejercicio de Evaluación de Investigación 2014 del Comité de Subvenciones Universitarias de Hong Kong, y está clasificada como la mejor universidad joven del mundo en el Ranking de Universidades Jóvenes de Times Higher Education 2020. Sus graduados ocuparon el décimo puesto mundial y el primero en Gran China en la Encuesta Global de Empleabilidad Universitaria 2019.
Sobre el CNIO
El CNIO (www.cnio.es) es una institución pública española dedicada a la investigación, diagnóstico y tratamiento del cáncer, adscrita al Instituto de Salud Carlos III (Ministerio de Ciencia e Innovación). Situado entre los 10 primeros centros monográficos de investigación del cáncer en el mundo (informe Scimago; Nature Index), el CNIO cubre todo el recorrido de la I+D+i, desde la investigación básica hasta la clínica, para trasladar los resultados de forma rápida y eficiente al Sistema Nacional de Salud y al mercado farmacéutico y biotecnológico.
El CNIO cuenta con un Programa de Terapias Experimentales que cubre las fases iniciales del desarrollo de fármacos dirigidos contra las dianas terapéuticas en las que trabajan sus científicos. Algunas de las moléculas del CNIO se han licenciado a empresas farmacéuticas internacionales. Además, el CNIO tiene una importante participación en programas de ‘open innovation’ de empresas farmacéuticas internacionales, lo que ha redundado en la entrada de más de 25 millones de euros al CNIO en los últimos 6 años. Finalmente, del CNIO se han generado 3 compañías spin-off, que también han conseguido hacer llegar a los pacientes los desarrollos del centro. Estos datos reflejan la apuesta de la Institución por la innovación y la transferencia de tecnología e ilustran la importancia de la colaboración público-privada para el avance en el diagnóstico y tratamiento de la enfermedad.
Artículo de referencia: MGMT genomic rearrangements contribute to chemotherapy resistance in gliomas. Barbara Oldrini et al (Nature Communications, 2020). DOI: 10.1038/s41467-020-17717-0
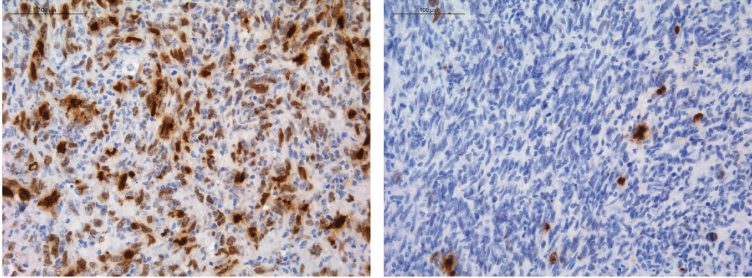
Células de glioma (en azul) bajo tratamiento con temozolomida, con daño en el ADN marcado en color marrón. Cuando el locus de MGMT está intacto, su expresión se silencia y la temozolomida promueve el daño del ADN en todas las células tumorales (izquierda); Cuando se reorganiza el locus de MGMT, las células de glioma sobreexpresan MGMT, pueden reparar el daño y seguir creciendo (derecha). /CNIO